Scandium, Sc, Ordnungszahl 21
Allgemeines
Scandium (von lat. Scandia „Skandinavien“) ist ein chemisches Element mit dem Symbol Sc und der Ordnungszahl 21.
Im Periodensystem steht es in der 3. Nebengruppe (Gruppe 3) oder Scandiumgruppe. Das weiche, silberweiße Element ist das erste der Übergangsmetalle und wird auch den Metallen der Seltenen Erden zugerechnet.

Scandium Metall
Scandium wurde 1879 von Lars Fredrik Nilson entdeckt. Aus 10 kg Euxenit und Gadolinit isolierte er ein Oxid mit bisher unbekannten Eigenschaften. Das von ihm vermutete neue Element nannte er zu Ehren seiner Heimat „Scandium“. Schon 1869 sagte Dmitri Iwanowitsch Mendelejew ein Element Eka-Bor mit der Ordnungszahl 21 voraus. Erst Per Teodor Cleve erkannte später die Übereinstimmung des Scandiums mit dem Eka-Bor.Reines Scandium wurde erstmals 1937 elektrolytisch aus einer eutektischen Schmelze aus Kalium-, Lithium- und Scandiumchlorid bei 700 bis 800 °C hergestellt.
Scandium gehört zu den seltenen Elementen. Elementar kommt es nicht vor, nur in einigen seltenen Mineralien findet man es in angereicherter Form:
Thortveitit: (Sc,Y)2Si2O7
Euxenit: (Y,Ca,Ce,U,Th)(Nb,Ta,Ti)2O6
Gadolinit Y2Fe2+Be2Si2O10
Ixiolit: (Ta,Nb,Sn,Mn,Fe)4O8
Bazzit: (Sc,Al)2Be3Si6O18
Kolbeckit: ScPO4 · 2 H2O
Periodensystem-scandium-21
Scandium findet sich in geringer Konzentration in über 800 Mineralien. Es ist daher auch in Erzkonzentraten der Übergangsmetalle als „Verunreinigung“ enthalten. Hierzu zählen russische und chinesische Wolframit- und Tantalitkonzentrate. Auch bei der Aufbereitung uranhaltiger Erze fallen Scandiumverbindungen an.
Die blaue Färbung des Aquamarins, einer Spielart des Berylls, soll durch Sc3+-Ionen verursacht werden.
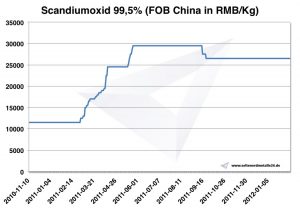
Chart Scandiumoxid 2010-2012
Gewinnung
Als Ausgangsstoff dient hauptsächlich Thortveitit, das in mehreren Verfahrensschritten zum Scandiumoxid aufbereitet wird. Metallisches Scandium wird anschließend durch Umsetzung zum Fluorid und Reduktion mit Calcium erzeugt.
Besonderheiten
Aufgrund seiner Dichte zählt Scandium zu den Leichtmetallen. An Luft wird es matt, es bildet sich eine schützende gelbliche Oxidschicht. Scandium reagiert mit verdünnten Säuren unter Bildung von Wasserstoff und dreiwertigen Kationen. In Wasserdampf erfolgt ab 600 °C die Umsetzung zu Scandiumoxid Sc2O3. In wässrigen Lösungen verhalten sich Sc-Kationen ähnlich wie Aluminium, was bei analytischen Trennungen oftmals Schwierigkeiten bereitet. In einer Mischung aus Salpetersäure und 48 % Fluorwasserstoff soll es beständig sein.
Verwendung
Seine Hauptanwendung findet Scandium als Scandiumiodid in Hochleistungs-Hochdruck-Quecksilberdampflampen, beispielsweise zur Stadionbeleuchtung. Zusammen mit Holmium und Dysprosium entsteht ein dem Tageslicht ähnliches Licht. Scandium wird auch zur Herstellung von Laserkristallen verwendet. Magnetischen Datenspeichern wird Scandiumoxid zur Erhöhung der Ummagnetisierungsgeschwindigkeit zugesetzt. Scandium als Scandiumchlorid wird in Mikromengen als ein sehr wichtiger Bestandteil im Katalysator bei der Chlorwasserstoffherstellung eingesetzt.
Als Legierungszusatz zeigt Scandium gefügestabilisierende und korngrößenfeinende Effekte. Eine Aluminium-Lithium-Legierung mit geringem Scandiumzusatz wird zur Herstellung einiger Bauteile in russischen Kampfflugzeugen verwendet. Auch in der modernen Fahrradindustrie (siehe Rennrad) werden Scandiumlegierungen eingesetzt. Diese Legierungen enthalten ebenfalls nur relativ wenig Scandium.
Scandiumpulver ist brennbar und daher als feuergefährlich einzustufen.
| Allgemein | |
| Name, Symbol
Ordnungszahl |
Scandium, Dc, 21 |
| Serie | Übergangsmetalle |
| Gruppe, Periode, Block | 3, 4, d |
| Aussehen | silbrig weiß |
| CAS-Nummer | 7440-20-2 |
| Massenanteil an der Erdhülle | 5,1 ppm |
| Atomar | |
| Atommasse | 44,955910 u |
| Atomradius | 160 pm |
| Kovalenter Radius | 170 pm |
| Elektronenkonf. | [Ar] 3d(1) 4s2 |
| 1. Ionisierungsenergie | 633,1 KJ/mol |
| 2. Ionisierungsenergie | 1235,0 KJ/mol |
| 3. Ionisierungsenergie | 2388,6 KJ/mol |
| Physikalisch | |
| Aggregatszustand | fest |
| Kristallstruktur | hexagonal |
| Dichte | 2,985 g/cm3 |
| Magnetismus | paramagnetisch (χm = 2,6 * 10(-4)) |
| Schmelzpunkt | 1814 K (1541 C) |
| Siedepunkt | 3103 K (2830 C) |
| Molares Volumen | 15,00 * 10(-6)m(3)/mol |
| Verdampfungswärme | 318 KJ/mol |
| Schmelzwärme | 16,0 KJ/mol |
| Elektrische Leitfähigkeit | 1,81*10(6) A/(V*m) |
| Wärmeleitfähigkeit | 16 W/(m*K) |